12月18日,由蘇州工業(yè)園區(qū)領(lǐng)先創(chuàng)新藥企信達(dá)生物與中國(guó)內(nèi)分泌和代謝領(lǐng)域的權(quán)威專(zhuān)家、頂尖科研機(jī)構(gòu)共同合作的瑪仕度肽兩項(xiàng)Ⅲ期臨床研究成果,登上國(guó)際科學(xué)頂級(jí)學(xué)術(shù)期刊《自然》(Nature)。該成果不僅是《自然》創(chuàng)刊以來(lái)首次在代謝內(nèi)分泌領(lǐng)域背靠背發(fā)表兩項(xiàng)Ⅲ期臨床研究,更使瑪仕度肽成為全球唯一同時(shí)登頂《自然》與《新英格蘭醫(yī)學(xué)雜志》(NEJM)的GLP-1類(lèi)藥物,彰顯中國(guó)在代謝疾病治療領(lǐng)域的原始創(chuàng)新能力與臨床研究實(shí)力。


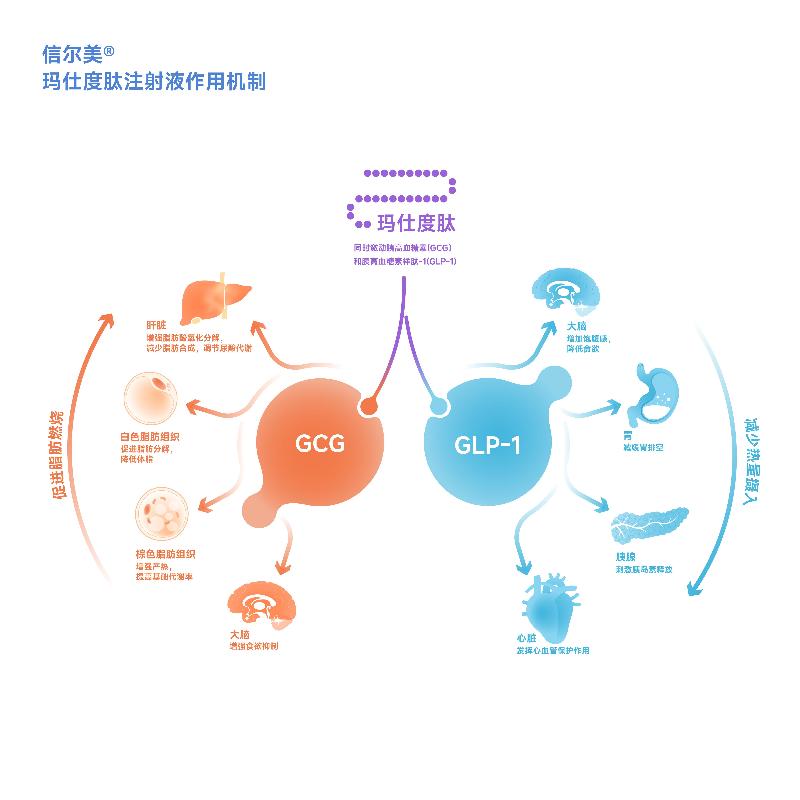
作為全球首個(gè)且唯一獲批的GCG/GLP-1天然雙靶點(diǎn)減重降糖藥物,瑪仕度肽針對(duì)中國(guó)患者代謝特征實(shí)現(xiàn)精準(zhǔn)突破。我國(guó)是糖尿病和肥胖大國(guó),患者群體普遍存在胰島素抵抗、脂肪肝及內(nèi)臟脂肪堆積等特征,但臨床長(zhǎng)期缺乏適配中國(guó)患者的用藥方案。此次發(fā)表的DREAMS-1(單藥治療2型糖尿病)與DREAMS-2(聯(lián)合口服降糖藥)兩項(xiàng)研究,均基于中國(guó)患者的臨床數(shù)據(jù),證實(shí)瑪仕度肽在血糖控制和減重療效均顯著優(yōu)于安慰劑或度拉糖肽(1.5mg),同時(shí)可改善多項(xiàng)心血管代謝、肝臟和腎臟相關(guān)指標(biāo),且耐受性良好,安全性特征與既往研究一致,未發(fā)現(xiàn)新增風(fēng)險(xiǎn)信號(hào)。
目前,瑪仕度肽已在中國(guó)獲批用于糖尿病和減重兩項(xiàng)適應(yīng)癥,并已開(kāi)展七項(xiàng)Ⅲ期研究,涵蓋糖尿病、肥胖及相關(guān)并發(fā)癥領(lǐng)域,在青少年肥胖人群中的Ib期臨床研究已達(dá)成主要終點(diǎn),結(jié)果顯示該藥物可為青少年帶來(lái)減重和多重代謝獲益。據(jù)悉,瑪仕度肽的青少年肥胖Ⅲ期注冊(cè)研究將于近期啟動(dòng),這也是中國(guó)首個(gè)針對(duì)青少年減重的Ⅲ期臨床。此外,國(guó)家藥監(jiān)局已受理瑪仕度肽9mg用于成人體重控制的上市申請(qǐng),將為大基數(shù)肥胖人群提供個(gè)性化且無(wú)創(chuàng)減重的新選擇。
此次成果發(fā)布,既是中國(guó)內(nèi)分泌和代謝領(lǐng)域原創(chuàng)性臨床研究的里程碑,更標(biāo)志著我國(guó)從“跟跑”到“領(lǐng)跑”的科研能力躍升。研究團(tuán)隊(duì)匯聚國(guó)內(nèi)多位代謝內(nèi)分泌權(quán)威專(zhuān)家,通過(guò)嚴(yán)謹(jǐn)規(guī)范的研究設(shè)計(jì)、權(quán)威的臨床解讀,確保了結(jié)論的科學(xué)性、規(guī)范性與臨床應(yīng)用價(jià)值。隨著瑪仕度肽在糖尿病、減重雙適應(yīng)癥的獲批及更多臨床數(shù)據(jù)的積累,中國(guó)創(chuàng)新藥企正以原始創(chuàng)新突破,為全球代謝疾病患者提供更優(yōu)解決方案,書(shū)寫(xiě)健康中國(guó)建設(shè)的嶄新篇章。
編輯 朱佳琪
2025年12月18日